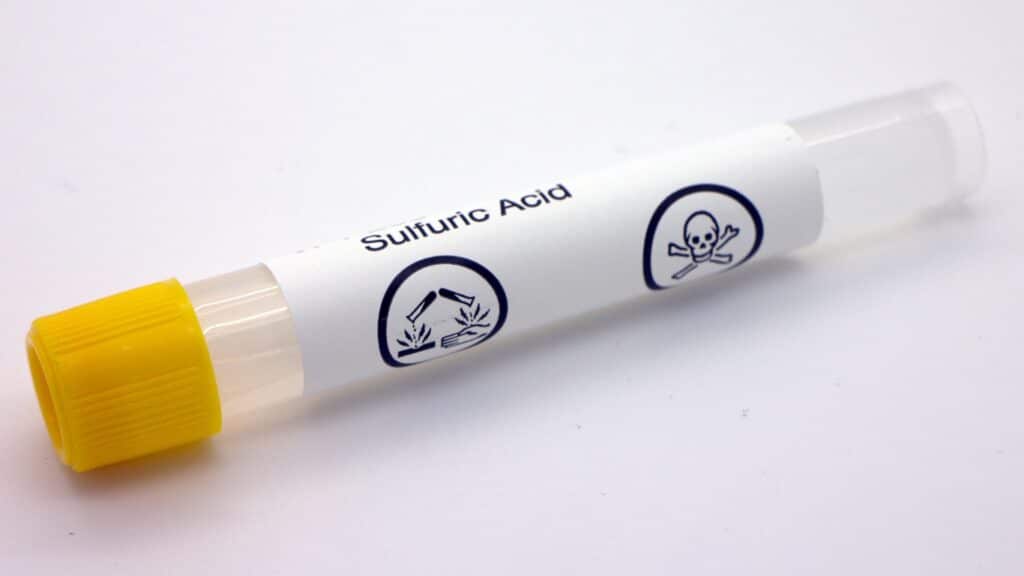
L’acide sulfurique (H2SO4) est l’un des composés chimiques les plus importants et les plus largement utilisés dans l’industrie moderne. Découvert au 8ème siècle par l’alchimiste Jabir ibn Hayyan, cet acide fort, incolore et inodore, joue un rôle crucial dans de nombreux processus industriels et applications quotidiennes. Avec une production annuelle mondiale dépassant les 260 millions de tonnes, l’acide sulfurique est un pilier de l’industrie chimique, intervenant dans la fabrication de fertilisants, le raffinage du pétrole, le traitement des métaux, et bien d’autres domaines.
Cet article explore en profondeur les multiples facettes de l’acide sulfurique, de ses propriétés physico-chimiques uniques à ses diverses applications industrielles. Nous examinerons également les précautions essentielles pour sa manipulation sécurisée, son impact environnemental, et les innovations récentes liées à son utilisation. Que vous soyez un professionnel de l’industrie, un étudiant en chimie, ou simplement curieux de comprendre l’importance de ce composé omniprésent, cet article vous fournira une vue d’ensemble complète et détaillée de l’acide sulfurique et de son rôle dans notre monde moderne.
Ce qu’il faut retenir
Voici les trois points les plus importants à retenir de cet article sur l’acide sulfurique :
- Polyvalence et importance industrielle : L’acide sulfurique est un composé chimique essentiel dans de nombreux secteurs industriels, notamment la production de fertilisants, le raffinage du pétrole, et la fabrication de nombreux autres produits chimiques. Sa production massive (plus de 260 millions de tonnes par an) témoigne de son rôle crucial dans l’économie mondiale.
- Propriétés uniques et réactivité : Les caractéristiques physico-chimiques de l’acide sulfurique, telles que son fort pouvoir déshydratant, ses propriétés oxydantes, et sa réactivité avec les métaux, en font un composé extrêmement versatile mais aussi potentiellement dangereux. La compréhension de ces propriétés est essentielle pour son utilisation sûre et efficace.
- Sécurité et gestion environnementale : La manipulation de l’acide sulfurique nécessite des précautions strictes en raison de sa nature corrosive et réactive. L’utilisation d’équipements de protection appropriés, le respect des procédures de stockage et de manipulation, ainsi que la prise en compte de son impact environnemental sont cruciaux pour une utilisation responsable de ce produit chimique puissant.
Ces points soulignent l’importance de l’acide sulfurique dans notre société industrielle moderne, tout en mettant l’accent sur la nécessité d’une gestion prudente et éclairée de ce composé chimique.
Caractéristiques principales :
- Formule chimique : H2SO4
- Masse molaire : 98,079 g/mol
- Densité : 1,8302 g/cm³ (à 20°C, pour l’acide concentré)
- Point d’ébullition : 337°C (acide concentré)
- Point de fusion : 10°C (acide concentré)
- Numéro CAS : 7664-93-9
1. Principales utilisations de l’acide sulfurique

L’acide sulfurique trouve son utilité dans une multitude de domaines, témoignant de sa versatilité et de son importance dans l’industrie moderne.
1.1 Fabrication de fertilisants
L’industrie des engrais consomme environ 60% de la production mondiale d’acide sulfurique. Son rôle est crucial dans la production de :
- Phosphate d’ammonium
- Superphosphate simple et triple
- Sulfate d’ammonium
Processus clé : La réaction de l’acide sulfurique avec la roche phosphatée produit de l’acide phosphorique, précurseur essentiel des engrais phosphatés.
1.2 Industrie pétrolière et raffinage
Dans le secteur pétrolier, l’acide sulfurique remplit plusieurs fonctions essentielles :
- Alkylation : Processus utilisant l’acide sulfurique comme catalyseur pour produire des essences à haut indice d’octane.
- Désulfuration : Élimination du soufre des produits pétroliers pour réduire les émissions polluantes.
- Traitement des boues : Séparation des émulsions eau-huile dans les résidus de raffinage.
1.3 Production de produits chimiques
L’acide sulfurique est un composant clé dans la synthèse de nombreux autres produits chimiques, notamment :
- Acide nitrique (HNO3)
- Acide chlorhydrique (HCl)
- Acide phosphorique (H3PO4)
- Sulfate d’aluminium (Al2(SO4)3), utilisé dans le traitement de l’eau
- Détergents et tensioactifs
1.4 Traitement des eaux
Dans le domaine du traitement des eaux, l’acide sulfurique joue un rôle crucial :
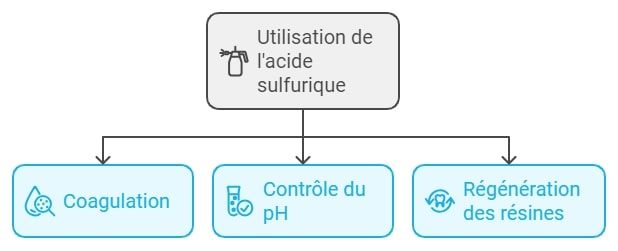
- Coagulation : Aide à la formation de flocs pour éliminer les particules en suspension.
- Contrôle du pH : Ajustement précis de l’acidité pour optimiser les processus de traitement.
- Régénération des résines échangeuses d’ions : Utilisé dans les systèmes d’adoucissement de l’eau.
1.5 Industrie du papier
L’acide sulfurique intervient dans la production de certains types de papier, notamment :
- Le papier sulfite, utilisé pour les emballages alimentaires et les papiers fins.
- Le traitement de la cellulose pour la production de viscose et de fibres textiles.
1.6 Métallurgie et traitement des métaux
- Décapage : Élimination des oxydes métalliques de la surface des métaux.
- Électrolyse : Utilisé dans la production et la purification de métaux comme le cuivre et le zinc.
- Batteries au plomb-acide : Composant essentiel de l’électrolyte dans ces batteries largement utilisées.
2. Propriétés physico-chimiques de l’acide sulfurique
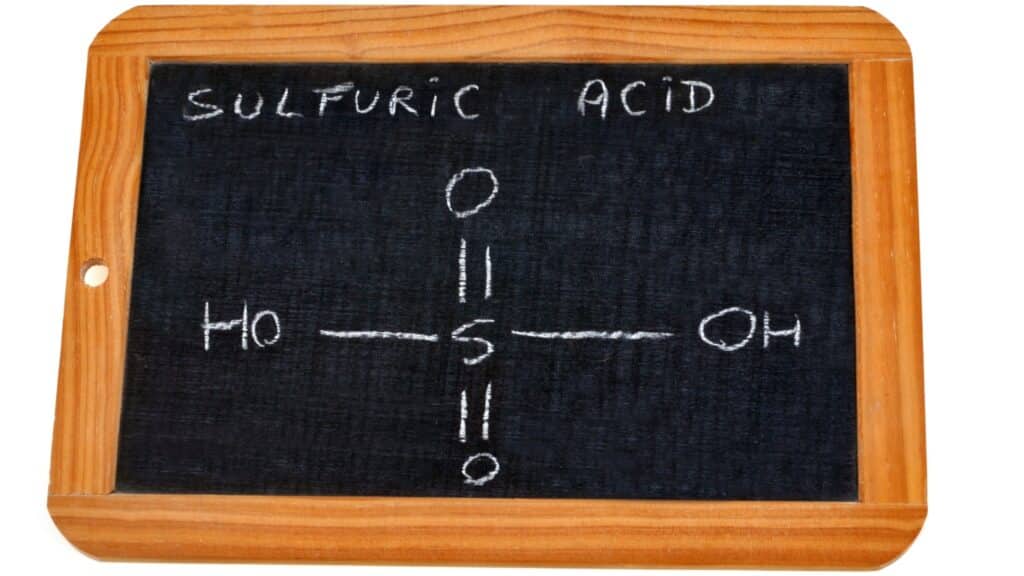
L’acide sulfurique possède des propriétés uniques qui expliquent son importance dans l’industrie.
2.1 Capacité déshydratante
L’acide sulfurique est un puissant agent déshydratant, avec une enthalpie de dilution de -880 kJ/mol.
Applications :
- Séchage des gaz industriels
- Déshydratation de composés organiques (ex : conversion de l’éthanol en éthylène)
- Agent desséchant dans les dessiccateurs de laboratoire
2.2 Pouvoir oxydant
L’acide sulfurique concentré est un oxydant puissant, avec un potentiel standard de réduction de 0,17 V.
Réactions notables :
- Oxydation du cuivre : Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
- Oxydation du carbone : C + 2H2SO4 → CO2 + 2SO2 + 2H2O
2.3 Réactivité avec les métaux
La réactivité de l’acide sulfurique avec les métaux dépend de sa concentration et de la nature du métal.
Série électrochimique : Les métaux situés au-dessus de l’hydrogène dans la série électrochimique réagissent avec l’acide sulfurique dilué pour produire de l’hydrogène.
2.4 Propriétés acido-basiques
L’acide sulfurique est un acide fort diprotique :
- Première constante d’acidité (Ka1) : très élevée (considérée comme infinie en solution aqueuse)
- Deuxième constante d’acidité (Ka2) : 1,2 × 10⁻²
| Concentration (%) | Densité (g/cm³ à 20°C) | Point d’ébullition (°C) | Viscosité (mPa·s à 20°C) |
|---|---|---|---|
| 10 | 1.066 | 102 | 1.20 |
| 50 | 1.395 | 124 | 3.10 |
| 98 | 1.8302 | 337 | 24.50 |
3. Précautions pour manipuler l’acide sulfurique en toute sécurité

La manipulation de l’acide sulfurique nécessite des précautions strictes en raison de sa nature corrosive et réactive.
3.1 Équipements de protection individuelle (EPI)
Normes de sécurité :
- Gants : EN 374 (protection contre les produits chimiques)
- Lunettes : EN 166 (protection contre les projections de liquides)
- Vêtements : EN 13034 (protection contre les produits chimiques liquides)
3.2 Environnement de travail
Systèmes de sécurité :
- Douches de sécurité : ANSI Z358.1
- Ventilation : ASHRAE Standard 62.1
3.3 Stockage sécurisé
Compatibilité des matériaux :
- Acier inoxydable 316L pour le stockage à long terme
- Polyéthylène haute densité (PEHD) pour les contenants de laboratoire
3.4 Procédures d’urgence
Premiers secours :
- Utiliser une solution de bicarbonate de sodium pour neutraliser les éclaboussures sur la peau
- Rinçage oculaire : solution saline isotonique recommandée
3.5 Formation et sensibilisation
Réglementation :
- REACH (Enregistrement, évaluation, autorisation et restriction des substances chimiques) en Europe
- OSHA (Occupational Safety and Health Administration) aux États-Unis
| Matériau | Compatibilité avec H2SO4 dilué | Compatibilité avec H2SO4 concentré |
|---|---|---|
| Acier inoxydable 316L | Excellente | Bonne |
| Polyéthylène haute densité (PEHD) | Excellente | Excellente |
| Verre borosilicaté | Excellente | Excellente |
| Acier au carbone | Mauvaise | Mauvaise |
| Aluminium | Mauvaise | Mauvaise |
4. Impact environnemental et développement durable
4.1 Effets sur l’environnement
L’acide sulfurique peut avoir des impacts significatifs sur l’environnement :
- Pluies acides : L’oxydation du dioxyde de soufre dans l’atmosphère produit de l’acide sulfurique, contribuant aux pluies acides.
- Acidification des sols et des eaux : Des déversements peuvent altérer gravement les écosystèmes.
4.2 Initiatives de développement durable
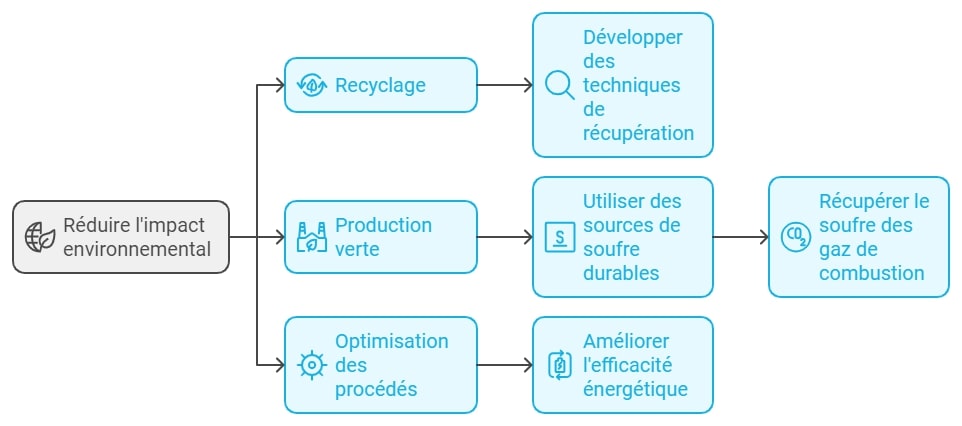
L’industrie cherche à réduire l’empreinte environnementale de la production et de l’utilisation de l’acide sulfurique :
- Recyclage : Développement de techniques pour récupérer et réutiliser l’acide sulfurique dans les processus industriels.
- Production verte : Utilisation de sources de soufre plus durables, comme la récupération du soufre des gaz de combustion.
- Optimisation des procédés : Amélioration de l’efficacité énergétique dans la production d’acide sulfurique.
5. Innovations et perspectives futures
5.1 Nouvelles applications
- Batteries au lithium-soufre : L’acide sulfurique pourrait jouer un rôle dans le développement de ces batteries à haute densité énergétique.
- Capture du CO2 : Utilisation potentielle dans les processus de captage et de stockage du carbone.
5.2 Recherche et développement
- Catalyse : Exploration de nouveaux catalyseurs pour améliorer l’efficacité des réactions impliquant l’acide sulfurique.
- Matériaux résistants : Développement de nouveaux matériaux plus résistants à la corrosion pour le stockage et le transport.
Conclusion
L’acide sulfurique reste un pilier de l’industrie chimique moderne, avec des applications qui continuent d’évoluer et de s’étendre. Sa production et son utilisation responsables, guidées par une compréhension approfondie de ses propriétés et des précautions nécessaires, sont essentielles pour exploiter pleinement son potentiel tout en minimisant les risques pour la santé et l’environnement. Alors que nous avançons vers un avenir plus durable, l’innovation dans l’utilisation et la gestion de l’acide sulfurique jouera un rôle crucial dans l’équilibre entre progrès industriel et préservation environnementale.